Hukum Kekekalan Massa (Lavoiser)
Hukum kekekalan Massa dikemukakan oleh Antoine Laurent
Lavoisier (1743-1794) yang berbunyi: ”Dalam suatu reaksi, massa zat
sebelum dan sesudah reaksi adalah sama”, dengan kata lain massa tidak
dapat diciptakan dan tidak dapat dimusnahkan. Artinya selama reaksi
terjadi tidak ada atom-atom pereaksi dan hasil reaksi yang hilang
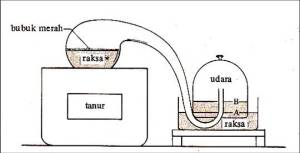
Percobaan yang dilakukan oleh Lavoisier.
Lavoisier mereaksikan cairan merkuri dengan gas oksigen dalam suatu
wadah di ruang tertutup sehingga menghasilkan merkuri oksida yang
berwarna merah. Apabila merkuri oksida dipanaskan kembali, senyawa
tersebut akan terurai menghasilkan sejumlah cairan merkuri dan gas
oksigen dengan jumlah yang sama seperti semula. Dengan bukti dari percobaan ini Lavoisier merumuskan suatu hukum
dasar kimia yaitu Hukum Kekekalan Massa yang menyatakan bahwa jumlah
massa zat sebelum dan sesudah rekasi adalah sama.
Pernyataan yang umum digunakan untuk menyatakan hukum kekekalan massa
adalah massa dapat berubah bentuk tetapi tidak dapat diciptakan atau
dimusnahkan. Untuk suatu proses kimiawi di dalam suatu sistem tertutup,
massa dari reaktan harus sama dengan massa produk.
Hukum kekekalan massa digunakan secara luas dalam bidang-bidang seperti kimia, teknik kimia, mekanika, dan dinamika fluida.
Hukum kekekalan massa dapat terlihat pada reaksi pembentukan hidrogen
dan oksigen dari air. Bila hidrogen dan oksigen dibentuk dari 36 g air,
maka bila reaksi berlangsung hingga seluruh air habis, akan diperoleh
massa campuran produk hidrogen dan oksigen sebesar 36gr. Bila reaksi
masih menyisakan air, maka massa campuran hidrogen, oksigen dan air yang
tidak bereaksi tetap sebesar 36gr.
Begitu juga kalau kita membakar kayu misalnya kayu korek api. Berlaku
juga hukum kekekalan massa. Memang setelah kayu terbakar akan menjadi
abu. Namun yang perlu anda ketahui adalah bahwa selain abu, pada
pembakaran kayu juga dihasilkan oksida karbon, asap dan uap air. Oksida
carbon dan uap air tidak tampak oleh mata karena bermujud gas. Jika
ditimbang ulang :
mk massa kayu + masa oksigen = masa abu + massa oksida karbon + massa uap air + massa asap.
Kalau hukum kekekalan massa memang benar, maka massa dari materi yang ada didunia ini berarti tidak pernah berubah.Kalau
begitu, maka ketika mahluk hidup, hewan, tumbuhan dan manusia, setiap
kali tumbuh menjadi semakin besar, berarti ada penambahan massa yang
diambilkan dari massa materi yang lain. Begitu juga setiap bayi yang
lahir, berarti ada energi dan massa di alam semesta ini yang beralih ke
dalam diri bayi.
Kalau kita makan, maka ada beberapa massa dari air dan makanan yang
makan akan menjadi daging pada tubuh kita. Kalau manusia bertambah
banyak, sesungguhnya tidak ada perubahan massa di alam semesta ini,
karena jumlah massa tentu juga sama sebagaimana jumlah energi di alam
semesti ini, berarti selalu sama.
Hukum Kekekalan Massa:
“massa zat sebelum reaksi sama dengan massa zat setelah reaksi”
Contoh :
S(s) + O2(g) → SO2(g)
1 mol S bereaksi dengan 1 mol O2 membentuk 1 mol SO2. 32 gram S bereaksi dengan 32 gram O2 membentuk 64 gram SO2. Massa total reaktan sama dengan massa produk yang dihasilkan.
H2(g) + ½ O2(g) → H2O(l)
1 mol H2 bereaksi dengan ½ mol O2 membentuk 1 mol H2O. 2 gram H2 bereaksi dengan 16 gram O2 membentuk 18 gram H2O. Massa total reaktan sama dengan massa produk yang terbentuk.
Contoh soal :
Pada wadah tertutup, 4 gram logam kalsium dibakar dengan oksigen,
menghasilkan kalsium oksida. Jika massa kalsium oksida yang dihasilkan
adalah 5,6 gram, maka berapa massa oksigen yang diperlukan?
Jawab :
m Ca = 4 gram
m CaO = 5,6 gram
m O2 = ..?
Berdasarkan hukum kekekalan massa :
Massa sebelum reaksi = massa sesudah reaksi
m Ca + m O2 = m CaO
m O2 = m CaO – m Ca
= (5,6 – 4,0) gram
= 1,6 gram
Jadi massa oksigen yang diperlukan adalah 1,6 gram.

